首页 学术动态
科研动态丨软物质物理与生物物理研究取得新进展
近日,物理科学与技术学院生物物理研究团队在软物质物理与生物物理方向取得新进展,多篇研究论文发表于自然系列期刊《Communications Biology》(影响因子 5.2,中科院一区),核酸系列顶刊《Nucleic Acids Research》(影响因子 13.1)和《Biophysical Journal》(影响因子 3.1)。
核小体是真核基因组的基本结构与功能单元,既承担 DNA 的压缩包装,也是染色质调控的关键枢纽,可与转录因子、染色质重塑复合体及多类表观遗传调控蛋白发生特异相互作用。核小体同时具有显著的动态性:离子微环境、癌相关组蛋白突变与翻译后修饰等因素,能够跨尺度重塑其结构稳定性、动力学行为与相互作用模式,进而影响染色质高级折叠与基因表达调控。系统解析核小体的动力学性质及其分子相互作用机制,对于理解基因表达与染色质重塑的物理基础,并揭示癌症等重大疾病的分子致病机制,具有重要科学意义与潜在应用价值。
在多种癌相关突变中,组蛋白变体H3.3的N端尾部G34R突变可见于儿童与成人胶质瘤以及骨肉瘤。既往研究提示该突变会影响表观基因组相关通路,但其对核小体背景下H3.3尾部结构与动态的影响仍缺乏深入认识。近期,彭云辉副研究员团队与加拿大女王大学Anna Panchenko教授、科罗拉多大学Catherine Musselman教授合作,结合核磁共振波谱与分子动力学模拟,研究核小体背景下 G34R突变对H3.3尾部的影响。结果显示,G34R突变会改变H3.3尾部的构象分布与动力学特征,并对尾部识别过程产生功能性影响;其中,突变降低了H3.3 在S31-K36区域的构象动态,并进一步改变整个尾部的构象分布。进一步的理论分析与实验表明,该类突变可通过重塑组蛋白尾部的构象统计特征及其与 DNA的结合模式分布,影响染色质重塑蛋白等调控因子的结合行为,从而可能调控染色质结构状态及基因表达(图1)。
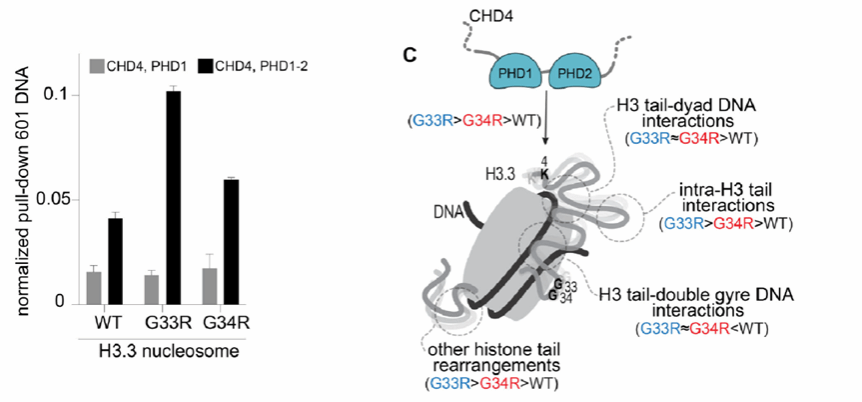
图1. H3.3 G34R突变调节组蛋白尾与DNA的结合模式、构象状态及 DNA 可及性,进而影响染色质重塑蛋白等调控因子的结合行为。
该研究成果以“G34R cancer mutation alters the conformational ensemble and dynamics of the histone H3.3 tails”为题,于2026年1月14日发表于《Nucleic Acids Research》。物理学院彭云辉副研究员为共同第一作者,2025级博士生张后芳为共同作者, 生物物理团队承担了全部理论计算工作。
连接组蛋白H1是介导核小体间相互作用并促进染色质高阶折叠的关键因子。已有研究表明,H1在多种肿瘤中存在频繁的体细胞突变,但这些突变如何在分子与物理层面改变H1的相互作用网络、结合稳定性及动力学过程,仍缺乏系统研究。由于H1具有较强的结构柔性,且其与DNA及多类调控蛋白形成复杂的相互作用网络,传统实验手段难以同时在原子尺度与网络层面解析其协同变化,从而限制了对H1突变致病机制的深入理解。
针对上述问题,研究团队整合结构数据与化学交联质谱数据,构建了以H1为核心的大规模相互作用网络,并结合癌症突变数据与分子动力学模拟,从网络到原子尺度系统分析突变对相互作用界面、网络拓扑性质及结构稳定性的影响(图2)。研究发现,H1癌症突变显著富集于蛋白结合界面及翻译后修饰位点,可通过改变局部理化性质并扰动修饰调控网络,重塑H1相互作用网络结构,并优先影响高连接度的关键枢纽节点。在原子尺度上,突变通过削弱H1-DNA相互作用并破坏关键氢键,显著降低H1-核小体复合体的结合稳定性。进一步构象分析表明,相关突变可诱导H1构象变化并增强其柔性,从而削弱其在染色质复合物中的结构支撑作用,降低整体稳定性。上述多重效应协同作用,最终可能破坏染色质高级结构组织并干扰表观遗传调控过程。
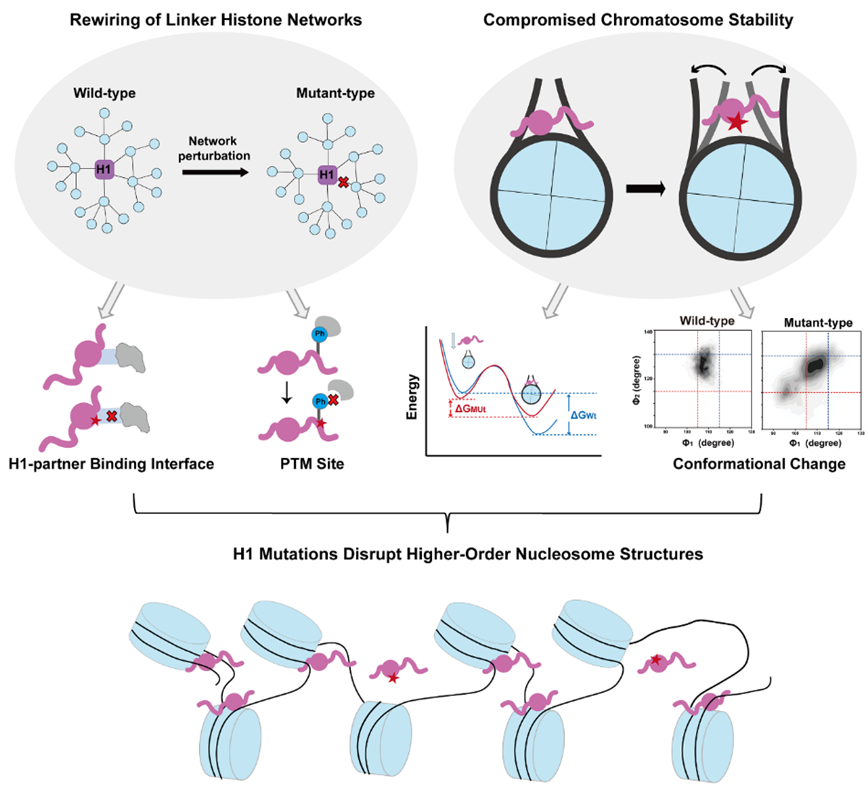
图2. 组蛋白H1突变通过重塑相互作用网络并降低H1-核小体复合物稳定性,进而导致染色质结构失调与表观遗传调控异常。
该研究成果以“Cancer mutations rewire linker histone interaction network and compromise chromatosome stability”为题,于2026年3月17日发表于《Biophysical Journal》。物理学院彭云辉副研究员为唯一通讯作者,物理学院2023级硕士生刘格格与2024级博士生胥旺为共同第一作者,华中师范大学为第一完成单位。
核小体中的组蛋白尾是内在的无序化蛋白,其结构高度动态且动力学行为十分复杂,传统的计算方法难以精确定量刻画其动力学行为;在实验上,则通常依赖核磁共振(NMR)进行表征。NMR 可通过残基特异性的自旋弛豫速率,反映分子在不同时间尺度上的运动特征。将分子动力学(MD)模拟与NMR弛豫测量相结合,对于验证力场、并更准确地描述生物分子(尤其是柔性或内在无序区域)的运动具有重要意义。然而,现有计算工具往往面向特定体系开发,或流程较为繁琐,缺乏对不同生物分子体系与模拟参数的通用适配性与灵活性,在计算生物分子动力学参数方面仍存在瓶颈。
针对上述问题,彭云辉副研究员团队与女王大学 Anna Panchenko 教授和伦敦大学学院卫铁军博士合作,开发了MD2NMR计算程序,实现了从分子动力学轨迹到 NMR弛豫参数的定量映射,建立了可将模拟结果与实验数据直接对比的生物大分子动力学表征框架(图3)。该程序采用高效算法计算偶极-偶极时间相关函数、谱密度函数与弛豫速率,并对整体旋转扩散与内部运动进行严格处理。MD2NMR支持多种轨迹格式,提供精细的参数控制,并兼容主流分子动力学软件。为验证方法的可靠性,团队选取多个特征明确的基准体系开展测试,将计算结果与实验数据对比后,结果显示该方法具有良好的一致性与可重复性。
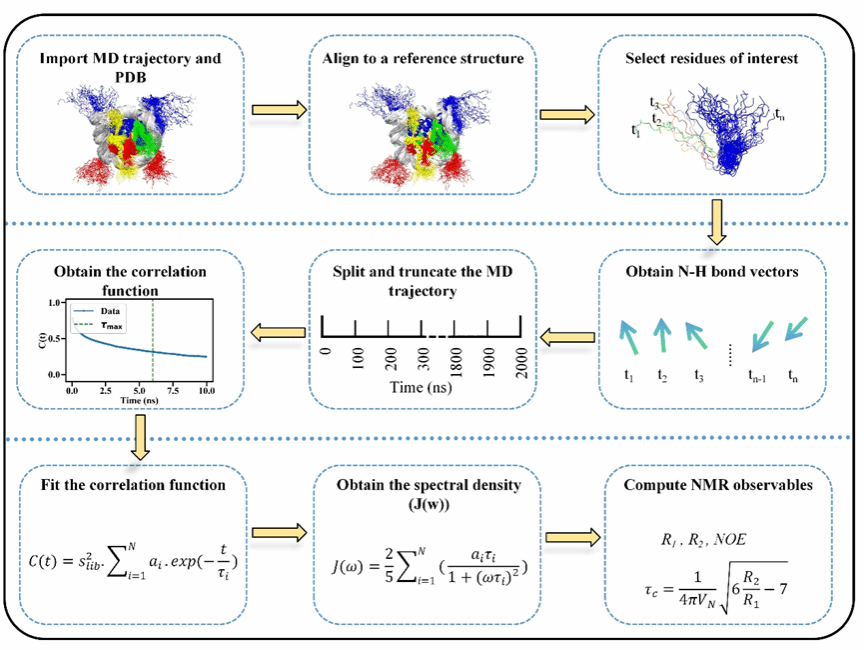
图3. MD2NMR工作流程示意图:从分子动力学轨迹出发,计算相关原子矢量的时间自相关函数,并通过多指数模型拟合获得谱密度函数;随后据此计算 NMR 弛豫参数,从而实现与实验NMR数据的直接比较。
该研究成果于2026年4月9日以“MD2NMR: linking molecular dynamics with NMR relaxation”为题发表于《Biophysical Journal》。物理学院彭云辉副研究员为该论文的唯一通讯作者,2025级博士生张后芳为共同第一作者,华中师范大学为第一完成单位。
二价阳离子在染色质结构维持及其功能调控中发挥重要作用。作为染色质的基本结构单元,核小体对离子微环境变化高度敏感,其结构与物理化学性质可受到显著影响。尽管单价盐离子对核小体动态结构调控的研究已相对丰富,但从原子尺度系统揭示二价阳离子与核小体相互作用机制的工作仍然不足,尤其是二价阳离子如何调控核小体结构与动力学过程的物理机制尚不清晰。由于核小体具有显著构象柔性,且组蛋白尾部与 DNA 之间存在复杂静电相互作用,传统实验手段难以解析离子结合引发的细微结构与动力学变化,从而限制了对离子介导染色质可及性调控机制的深入理解。
针对上述问题,研究团队基于全原子分子动力学模拟,系统分析了Mg²⁺与 Ca²⁺在核小体中的结合行为及其结构调控效应(图4)。结果表明,二价阳离子可通过屏蔽DNA超螺旋之间的静电排斥促进核小体整体构象收缩;结合杨氏模量计算与 DNA区域协同运动分析进一步发现,离子结合显著增强了核小体的机械刚性。与此同时,离子结合还明显削弱组蛋白尾部与DNA的相互作用,使H3尾部构象柔性增强,提示其构象动力学特征发生显著改变。总体而言,二价阳离子在增强核小体整体刚性的同时,促进组蛋白尾部由紧密结合态向高柔性状态转变,体现出“结构压缩与尾部柔性增强”的双重调控机制,为理解离子微环境变化如何影响基因可及性与染色质状态转换提供了分子层面的理论依据。
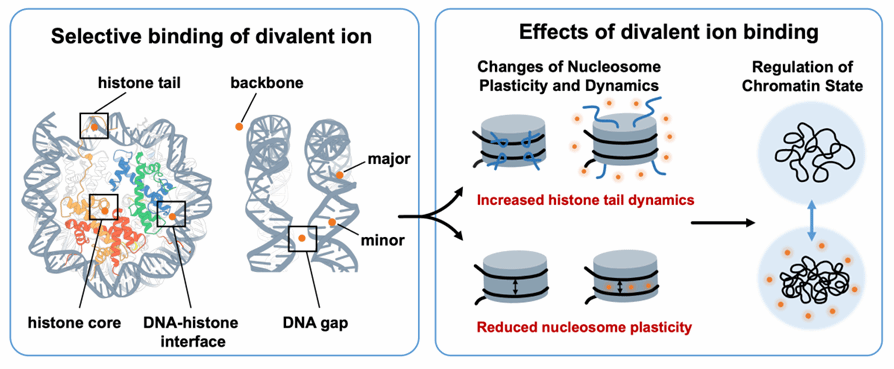
图4. 二价阳离子选择性结合重塑核小体力学性质与组蛋白尾部动力学,并可能影响染色质结构状态转变。
该研究成果于2026年2月5日以“Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics”为题发表于《Communications Biology》。物理学院彭云辉副研究员为该论文的唯一通讯作者,2023级硕士生胡冠华为第一作者,华中师范大学为第一完成单位。
上述研究工作得到了国家自然科学基金青年项目(C类)、武汉市自然科学基金(探索计划)以及华中师范大学中央高校基本科研业务费(基础研究交叉专项)的共同资助。
相关论文:
1. Harrison Fuchs, Yunhui Peng, Shine Ayyapan, Ruben Rosas, Houfang Zhang, Anna R. Panchenko, and Catherine A. Musselman. “G34R cancer mutation alters the conformational ensemble and dynamics of the histone H3. 3 tails”, Nucleic Acids Research 54, no. 2 (2026): gkaf1381. https://doi.org/10.1093/nar/gkaf1381
2. Gege Liu, Wang Xu, Guanhua Hu, Houfang Zhang, and Yunhui Peng. “Cancer mutations rewire linker histone interaction network and compromise chromatosome stability”, Biophysical Journal 125, (2026): 1415-1433. https://www.cell.com/biophysj/abstract/S0006-3495(26)00065-2
3. Houfang Zhang, Tiejun Wei, Anna R. Panchenko, Catherine A. Musselman, Yunhui Peng. “MD2NMR: linking molecular dynamics with NMR relaxation”,Biophysical Journal, 2026, In Press. https://doi.org/10.1016/j.bpj.2026.04.007
4. Guanhua Hu, Houfang Zhang, Wang Xu, Gege Liu, and Yunhui Peng. “Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics”, Communications Biology 9 (2026): 365. https://www.nature.com/articles/s42003-026-09648-1



